Retinosis Pigmentaria, Alternativas para la Rehabilitación Visual
Por Lizhbet Natalie del Pilar Melo Torres, Tecnólogo Médico en Oftalmología y alumna del Máster en Optometría Clínica y Terapia Visual
Resumen
La retinosis pigmentaria es una enfermedad genética en la que el afectado pierde progresivamente su visión, cursa con discapacidad visual que finalmente desencadena ceguera, lo que repercute directamente en sus relaciones sociales, autonomía, salud mental y calidad de vida. La rehabilitación visual tiene como objetivo ofrecer herramientas al afectado para mejorar su autonomía personal. Las ayudas ópticas son las herramientas por excelencia para mejorar la calidad de vida de los pacientes a través de las mejoras en la agudeza visual. Contando en la última década con avances tales como las prótesis retinal. El propósito de este estudio es determinar a través de la revisión bibliográfica la alternativa más conveniente para el paciente.
Material y métodos: Este es un estudio retrospectivo basado en la revisión bibliográfica de estudios entre 2010 y 2017 de portales web tales como PubMed y Google Académico.
Resultados: Las ayudas ópticas electrónicas han variado en sus especificaciones técnicas en la última década, siendo las prótesis retinales como Alpha AMS y Argus II las que han demostrado grandes avances en el restablecimiento de la visón.
Conclusión: Las recomendaciones entregadas al paciente y sus familiares deben tomarse en base al conocimiento científico adquirido en cuanto a seguridad, eficiencia de las distintas alternativas, estado actual e historia natural de la enfermedad así como las necesidades personales del paciente.
La retinosis pigmentaria (RP) es una enfermedad congénita degenerativa de los fotorreceptores de la retina, de carácter crónico y progresivo, que puede presentarse de manera aislada o como parte de un grupo de enfermedades. Constituye la primera causa de ceguera en la población adulta y su prevalencia a nivel mundial es de 1 en 4000 personas. Inicialmente los bastones son los primeros en afectarse, estos abundan en la retina periférica y son los encargados de la visión nocturna, periférica y blanco-negro.
Dentro de sus signos podemos apreciar al fondo de ojo acúmulos de pigmento producto de la degeneración retinal (espículas óseas), atenuación del árbol vascular retiniano y cambios en la mácula. Los cambios maculares son usualmente vistos en etapas terminales mientras que las espículas óseas es el signo típico aún en etapas precoces.
De acuerdo al Servicio de Evaluación del Servicio Canario de la Salud (2017), el diagnóstico se realiza tras la evaluación de los síntomas, signos al fondo de ojo y el examen de Electrorretinograma (ERG) que concluirá en la disminución de las longitudes de onda atribuibles a un no funcionamiento de los fotorreceptores.
Las causas genéticas de la RP son bastante complejas ya que la misma enfermedad puede estar causada por mutaciones en uno de muchos genes implicados, existe una gran cantidad de mutaciones diferentes en cada gen que causan diferentes formas de la enfermedad y una misma mutación puede producir fenotipos diferentes. Puede ser heredada de forma autosómica dominante (20-25% de los casos), autosómica recesiva (15-20% de los casos) o ligada al cromosoma X (5-10% de los casos). No todas las formas hereditarias tienen la misma gravedad ni igual evolución sino que parece estar asociada a una cierta variabilidad clínica. No existe diferencia significativa en la prevalencia en relación al sexo. Y en lo que refiere a la clínica, la forma más severa corresponde al tipo ligada al cromosoma X (Trujillo et al., 2012).
No existe una clasificación única y generalizada para la RP, si bien la mayoría de los autores usan cuatro modalidades de clasificación (tabla 1) (García, Gil y Bambó, 2015).
Tabla 1. Clasificación de la Retinosis Pigmentaria
Clasificación teniendo en cuenta: | Tipos de Retinosis Pigmentaria |
Las características clínicas. | RP típica. RP atípica. RP asociada (RP sindrómica). |
La edad de comienza de la RP. | Comienzo precoz: antes de los 10 años. Comienzo juvenil: entre los 10 y 20 años. Comienzo tardío: después de los 21 años. |
El tipo de herencia de la RP | Autosómica recesiva. Autosómica dominante. Recesiva ligada al cromosoma X. Herencia no definida. |
El estadio clínico de la RP (se valora siempre el ojo que está mejor) | Estadio I: AV > 0,6 y CV ≥ 15° Estadio II: AV > 0,3 y CV entre 11° y 15° Estadio III: AV > 0,05 y CV entre 10° y 5° Estadio IV: AV > 0,05 y CV < 5° |
Abreviaturas: AV (agudeza visual); CV (campo visual).
Si bien es una patología congénita sus primeros síntomas y/o signos no suelen ser percibidos antes de la adolescencia. Por lo tanto la persona afectada no es consciente de su enfermedad hasta en fases avanzadas de la misma. Debido a la gran variabilidad genética sus manifestaciones clínicas pueden presentarse de forma diferentes, incluso entre individuos de una misma familia. Sin embargo las comunes son: Ceguera nocturna (nictalopía) o escasa adaptación a la oscuridad, disminución del campo visual (CV) iniciándose de manera irregular en la periferia, puede ser una pérdida progresiva concéntrica del CV, pérdida que se inicie en la parte superior y luego avanza hacia un escotoma arqueado o escotomas anulares y en etapas finales queda la visión en túnel. La visión central puede estar preservada en algunos casos y en otros puede llegar a la ceguera absoluta, ya que en la progresión de la enfermedad los conos son los siguientes afectados (Guía de Práctica Clínica para las Distrofias Hereditarias de Retina, 2017).
Lo que respecta a su AV podemos clasificar al paciente como baja visión o ceguera. Se considera baja visión como disminución de las funciones visuales, no recuperables por tratamiento. Aquí la AV está comprendida entre 0,05 y 0,3 en el mejor ojo y/o un CV inferior a 20° en el mejor ojo. El paciente mantiene una visión útil, a lo que se denomina remanente visual. El remanente visual puede ser mejorado o potenciado mediante la rehabilitación visual, con el fin de ayudar a la calidad de vida de los afectados. Por otro lado existe la ceguera, en donde los afectados cursan con una AV menor a 0,05 y /o un CV menor a 10°, en estos casos la rehabilitación visual es difícil de realizar, por lo que se debiera evaluar otras alternativas para recuperar la visión, como son las opciones de prótesis retinal (Latham, Baranian, Timmis, Fisher y Pardhan, 2017).
La deficiencia visual a causa de la RP resulta en una significativa desventaja económica y social en el afectado, su familia y a la sociedad en general. Estos pacientes acuden con mayor frecuencia al médico y generalmente necesitan asistencia para desarrollar sus actividades diarias. Uno de los objetivos a lograr de quienes sufren discapacidad visual, la movilidad es lo que les proporciona mayor desafío. Las mayores dificultades son en la orientación relacionadas con las condiciones de iluminación, evitando obstáculos y búsqueda de objetos. Actividades como salir de compras, realizar deporte o usar el transporte público son consideradas como limitaciones ante la falta de movilidad, pero también se deben considerar como actividades de la vida diaria y de interacción social por lo tanto resulta en una drástica reducción de su calidad de vida al comparar con la población de la misma edad (Latham et al, 2017).
De acuerdo a los estudios realizados por Kempen, Ballemans, Ranchor, Van Rens y Zijlstra (2012) y Latham et al. (2015) quienes padecen de una progresión de su discapacidad visual, como es el caso de la RP, tienen mayor riesgo de sufrir depresiones y cuadros de ansiedad. Este cambio en el estado emocional influye en su funcionamiento y/o desenvolvimiento en el espacio lo cual se relaciona con la calidad de vida.
Objetivo General: Determinar a través de la revisión bibliográfica las alternativas actuales para la Rehabilitación visual en pacientes afectados con Retinosis Pigmentaria.
Objetivos Específicos:
- Comprender las dificultades visuales y sociales de quienes padecen Retinosis Pigmentaria.
- Describir las utilidades de la prótesis retinal como nueva alternativa de tratamiento para restablecer la función visual en Retinosis Pigmentaria.
- Analizar el contexto sociocultural de los pacientes con Retinosis Pigmentaria en la actualidad.
En este estudio retrospectivo de corte transversal descriptivo, basado en la revisión bibliográfica para lo cual las plataformas consultadas fueron Google Académico y PubMed, páginas oficiales de la Organización Mundial de la Salud (OMS), Agencia Internacional de Prevención de la Ceguera (IAPB), Organización Retinosis Retina Besigare y Federación de Asociaciones de Retinosis Pigmentaria de España.
Se realizaron búsquedas bibliográficas a través de internet (español e inglés), sobre retinosis pigmentaria (definición, causas y tratamiento), rehabilitación visual (ayudas ópticas, no ópticas y prótesis retinal), baja visión y ceguera (definición, tratamiento y aspectos psicosociales). Los criterios utilizados para la selección de artículos científicos fueron aquellos que estuvieran publicados entre los años 2010 y 2017.
Sistema de Variables
Variables A B |
Dimensión |
Sub-dimensión en: |
Indicadores |
Determinar a través de la revisión bibliográfica las alternativas actuales para Rehabilitación Visual con pacientes afectados con Retinosis Pigmentaria | Dificultades sociales y visuales | – El trabajo – El hogar – La sociedad | Rehabilitación visual |
Ayudas ópticas | Lupas Microscopio Telescopio Electrónicas | ||
Prótesis Retinal | – Alpha IMS – Argus II |
Problemas de discapacidad visual son consulta frecuente en oftalmología. Los afectados de Retinosis Pigmentaria desean cada vez más conocer los aspectos inherentes a su enfermedad y a pesar de tener pronósticos desalentadores siempre están esperanzados en nuevos avances en la cura o rehabilitación visual disponible en el mercado.
Rehabilitación visual
Una vez que ha sido diagnosticada la enfermedad nos enfocaremos en la rehabilitación visual. Nuestro objetivo no es solo mejorar su calidad visual sino rehabilitar al paciente que depende de su función visual. Mediante diferentes técnicas, recursos, ayudas ópticas y ayudas adaptativas, buscamos lograr la autonomía e independencia de la persona con discapacidad (García-Martín, Gil-Arribas y Bambó-Rubio, 2015).
Para orientar de forma integral la rehabilitación debemos evaluar los cambios en la visión y cómo estos influyen en su vida cotidiana. Debemos explorar el campo visual, la adaptación al movimiento, calculo de distancias, sensibilidad al contraste, agudeza visual y motilidad ocular. En base a ello, evaluar las discapacidades que experimenta el paciente ante la ceguera nocturna o dificultades en la lectura. Conocer su repercusión psicológica de estos síntomas, ya que la rehabilitación será más exitosa cuando el paciente haya aceptado su condición y sus expectativas sean razonables (Escobar, Vélez y Barrera, 2017).
Ayudas ópticas.
La técnica utilizada mayormente son las ayudas ópticas cuyo objetivo es favorecer la utilización del remanente visual mediante el uso de sistemas ópticos. Su funcionamiento esta en producir una magnificación de la imagen en la retina, aumentando su rendimiento visual. La elección del tipo de ayuda óptica a utilizar dependerá del grado de afectación de campo visual y las necesidades del paciente. Tabla 2 (García et al., 2015).
Tabla 2. Clasificación de ayudas ópticas.
|
Tipo |
Características |
|
Lupa
Microscopio
Telescopio
Sistema electrónicos |
Para trabajos a corta distancia y de corta duración. Permite aumentar el tamaño de los objetos al mirar a través de ella. Cuanto mayor es la lupa, menor es la magnificación del campo visual. El campo visual aumenta a medida que el ojo se acerca más a la lente. Puede ser con mango, soporte o brazo flexible.
El material de lectura se acerca al ojo y se crea una imagen retiniana aumentada y clara. Cuando mayor es la ampliación, más pequeño es el CV y más corta la distancia de trabajo. Puede ser monocular y además montable en gafas
Se utiliza para distancias lejanas ya que aumenta el tamaño de la imagen. Desventaja la limitación del CV, genera la percepción de movimientos de los objetos y provoca cambio en la percepción espacial de los objetos.
Aumentar el tamaño de la imagen tras el uso de un circuito cerrado de TV. Permiten regular el contraste, iluminación y el brillo. Ofrecen un campo de lectura y una profundidad de campo superior versus a las otras ayudas ópticas |
Prótesis retinal
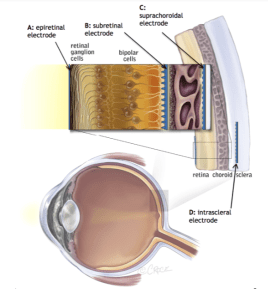
Los nuevos avances en medicina, cirugía y tecnológicos tienen como objetivo restaurar la pérdida de la función visual a través de dispositivos de visión artificial. La visión artificial puede ser implantada en diferentes localizaciones de la vía visual, dependiendo de la causa de la pérdida visual (retina, nervio óptico, núcleo geniculado lateral o cortex visual) (Daschner, Rothermel, Ralf, Rudort y Stett, 2018).
Para el caso de la RP nos referiremos a la implantación de tecnología a nivel de la retina: prótesis retinal.
El éxito de esta tecnología ha sido tal que actualmente se encuentran dispositivos disponibles comercialmente, el Argus II de Second Sight Medical Products, USA (aprobado en 2011) (Ayton et al., 2014), el Alpha IMS de Retina Implant AG (aprobado en 2011, actualmente discontinuado) (Daschner et al., 2018) y el Alpha AMS de Retina Implant AG, Germany (aprobado en 2016) (Ayton et al., 2014).
La percepción visual comienza con la luz pasando a través de la cornea y el cristalino hasta hacer foco en la retina. En la retina, los fotorreceptores absorben la luz visible y desencadenan la fototransducción, proceso que convierte la luz en una señal eléctrica. La señal eléctrica producida es procesada por las células neuronales de la retina (células bipolar, horizontal y amacrina) y enviada por las células ganglionares al núcleo geniculado lateral a través del nervio óptico y luego hacia el cortex visual (Brandli, Luu, Guymer y Ayton, 2016)
Estos dispositivos usan electrodos implantados entre o cerca de la retina con la intención de estimular la retina interna, eludiendo a los receptores no funcionales y estimulando la red celular restante de la retina. Luego utiliza la vía visual posterior intacta para transmitir la señal luminosa al cortex visual (Lewis y Rosenfeld, 2016). Es imprescindible que la capa interna de la retina se encuentre relativamente intacta, como es el caso de la RP, en donde la degeneración de los fotorreceptores ocurre en la capa externa de la retina. También, estos dispositivos asumen que la retina interna aún es capaz de procesar la información lumínica por lo que la estimulación eléctrica modulada de las células ganglionares aún puede actuar en la percepción visual (Zhang, 2016).
En la selección de candidatos a prótesis retinal, debemos considerar que la retina en etapas avanzadas de la enfermedad sufre una significativa reorganización y remodelación de su organización anatómica, receptora y funcional. Las células bipolares y amacrina sobreviven realizando sinapsis anormal y las células ganglionares disminuyen en un 30% (Cohen, 2018).
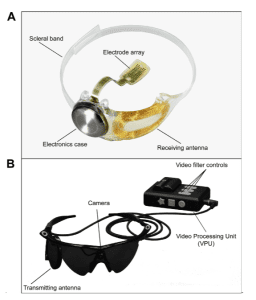
Prótesis Epiretinal Argus II
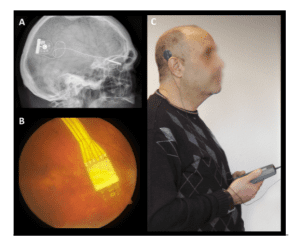
El dispositivo Argus II consiste en 60 electrodos ubicados en la membrana limitante interna de la retina, con la intención de estimular a las células ganglionares y las neuronas retinales internas. Los electrodos son conectados por cable a una unidad de video procesamiento ubicado en la esclera por fuera del globo ocular. El paciente es provisto de unos lentes con una pequeña cámara que le entrega datos a los electrodos (Ayton et al., 2014).
En el artículo Retinal Prosthesis System for Advanced Retinosis Pigmentos: a Health Technology Assessment (2016), la vídeo-cámara captura imágenes visuales y las convierte en pulsos de estimulación eléctricas en la unidad de vídeo-procesamiento. La unidad de vídeo-procesamiento transmite las imágenes de forma inalámbrica usando una antena. El implante emite pequeños impulsos eléctricos que estimulan a la retina interna eludiendo a las fotorreceptores dañados. Las células retinales ya estimuladas transmiten la información visual al cerebro a través del nervio óptico y luego la visión inducida es percibida como un patrón de luces en el córtex visual.
Es una buena opción en pacientes con RP puesto que aún mantienen visión residual y la retina aún puede responder a estímulos eléctricos. Tiene como ventaja que es poco invasivo a nivel retinal ya que no ocluye la vascularización retinal y es fácilmente monitoreado. Al tener un sistema de cámara externo ayuda a que la percepción de la imagen sea mejorada en contraste, detalles y magnificación (DaCruz et al., 2016).
Prótesis Subretinal Alpha AMS
El dispositivo Alpha IMS y AMS, se basan en 1500 fotodiodos ubicado en el espacio subretinal entre el epitelio pigmentario y la capa de fotorreceptores, por lo que los fotodiodos se encuentran muy próximos para activar a las células bipolar y amacrina. El implante consiste en un microchip MPDA y un cable para el suministro de energía y un control de señal que termina en una caja receptora pequeña ubicado tras la oreja. Un pequeño cable conecta el electrodo a la caja subdérmica. La luz del exterior es recibida por los fotodiodos para luego ser procesada y amplificada antes de ser enviada a los electrodos correspondientes. La combinación de fotodiodos y electrodos provee de estimulación punto a punto de las células bipolares de la retina, eliminando la necesidad de una cámara externa. Un aspecto positivo a comparar respecto a Argus II es que permite al paciente hacer uso de su propio sistema óptico para focalizar tras el uso natural del movimiento de los ojos permitiendo el rastreo del objeto mediante el movimiento sacádicos de los ojos y con el uso de las microsacadas logra refrescar la imagen en la retina (Stingl et al., 2015).
Un aspecto negativo a considerar es la durabilidad del dispositivo implantado ya que en pacientes implantados con Alpha IMS solo un 32% aún están en funcionamiento después de un año. Su sucesor Alpha AMS ha considerado esta desventaja y la han mejorado, con un 81% de funcionalidad después de un año (Ayton et al., 2014)
Evidencia clínica
Las necesidades de rehabilitación de un paciente con discapacidad visual varían considerablemente. El nivel de necesidad depende de la complejidad de los problemas, metas, estado psicosocial, los atributos personales y no solo del estado de la agudeza visual. Debemos reconocer el impacto que genera la pérdida parcial e irreversible de la visión y asegurarle al paciente una ayuda acertada a través de las alternativas actuales en el mercado (Kempen et al., 2012; Latham et al., 2017).
Existen variados estudios en los cuales se evidencia la efectividad de las ayudas ópticas y de las prótesis retinales, pero lamentablemente para ambos casos se utilizan test de evaluación y medidas distintas por lo que hacer un estudio comparativo utilizando los mismo test es de vital importancia. Algo en común entre las ayudas ópticas y la prótesis retinal es en la selección de pacientes. En ambos casos se debe tener una expectativa razonable, tener apoyo familiar, habilidades para relacionarse con el medio y buena salud oftalmológica (Latham et al., 2015).
Debemos iniciar con la medición de la calidad de vida que sufre los afectados. En la bibliografía consultada no se pudo contar con un único método estandarizado que fuese aplicado en todos los estudios de paciente con Retinosis Pigmentaria (Stingl et al., 2015)
El test Dutch ICF Activity Inventory (D-AI), es una adaptación del International Classificacion of Functioning, Disability and Health (ICF) desarrollado por la Organización Mundial de la Salud y que ha sido utilizado en varios estudios con la intención de comprender las mayores dificultades de los afectados en relación a su cuidado personal, aplicación de conocimientos, realizar actividades o tareas habituales, actividad social, relación familiar y salud mental. Gracias al test D-AI podremos establecer qué tipo de rehabilitación es útil para nuestro paciente de acuerdo a sus limitaciones y necesidades visuales para sus actividades diarias (Bruijning, Nispen y Rens, 2010).
El test Functional Low-Vision Observer Rated Assessment (FLORA) cuya intención es evaluar la funcionalidad de los tratamientos en discapacidad visual (Geruschat et al., 2015). Fue implementado por Ghodasra et al. (2016) para evaluar el impacto del implante Argus II en la vida diarias de los pacientes. Para este caso la experiencia fue positiva (80% de aceptación) pero aun así no se encontró comparación u aplicación del test en los estudios de Alpha IMS o en ayudas ópticas.
El estudio realizado por Azoulay et al. (2015), demuestra que existe interés en conocer la calidad de vida de quienes sufren discapacidad visual a causa de la RP. Para ello implementaron el test Item-25 del National Eye Instituye Visual Functioning Questionnaire (NEI-VFQ-25) y el cuestionario del Hospital de la Ansiedad y Depresión (HADS). NEI-VFQ-25 consiste en 25 preguntas diseñadas para evaluar la visión, distancia de visión, visión periférica, motilidad, visión a color, dolor ocular, limitaciones, dependencia, frustración social y salud mental. Hasta el momento es la mejor alternativa evaluada por FDA. HADS consiste en 14 preguntas para evaluar el nivel de depresión-ansiedad del afectado (Sugawara et al., 2010).
Otro ejemplo para evaluar la calidad de vida de quienes padecen RP es el estudio realizado por Levinson et al. (2017), en donde también recurrió al NEI-VFQ-25 y se complementó con el test Pepper Assessment Tool for Disability (PAT-D) y el test 36-Item Short For Health Survey (SF-36). PAT-D consiste en un cuestionario de 19 ítem para evaluar la movilidad, actividades de la vida diaria y actividades instrumentales del diario vivir. SF-36 que evalúa la salud en relación a la calidad de vida, funcionamiento físico, limitaciones debido a problemas de salud física, limitaciones debido a problemas de salud emocional, funcionamiento social, libertad de dolor, energía o fatiga, bienestar emocional y percepción general de salud.
Como hemos señalado, la progresión de la RP llevará al paciente a presentar visión túnel y a consecuencia dificultades en el desenvolvimiento, por lo que resulta de utilidad evaluar la habilidad de exploración y localización de objetos dentro y fuera del campo visual. Para ello AlSaqr y Dickinson (2016) han desarrollado el test Assessment of Visual Awareness (AVA). El test presenta varias limitaciones y no esta validado, pero este estudio nos demuestra que hay parámetros que debemos considerar al momento de evaluar que alternativas reales podemos ofrecer a los pacientes de acuerdo al estado actual de la enfermedad.
Una vez evaluada la calidad de vida del paciente y que se espera mejorar en ella debemos considerar evaluar la función visual que podemos obtener tras la rehabilitación visual. La función visual requiere un test de medida que incluya la agudeza visual, detección y localización de objetos y perspectivas del paciente.
La agudeza visual se estima en equivalente Snellen de 20/1250 para Argus II (1,80 logMAR) (Humayun, Eugene de Juan y Dagnelie, 2016) y de 20/546 para Alpha IMS (1,43 logMAR) (Stingl et al., 2015). Mientras que la percepción visual tras la utilización de los dispositivos de prótesis retinal se mide con Basic Assessment of Light and Motion (BaLM) (Humayun et al., 2016) test y Freiburg Visual Acuity Test (FrACT) (Lange, Feltgen, Junker, Schulze y Bach, 2009).
BaLM está desarrollado para medir cuatro dimensiones visuales: la percepción de la luz (presente/ausente), resolución (discriminación simple versus doble flash), localización de la luz y movimiento. Este test nos ofrece una cuantificación de la función visual haciendo diferencia entre no percepción de luz, percepción de luz y movimiento de mano (Bach, Wilke, Wilhelm, Zrenner y Wilke, 2010). FrACT se puede aplicar para cuantificar la agudeza visual mayor a movimiento de mano. El paciente se ubica a 50 cm de una pantalla y se presenta el C-Landolt, un anillo a la vez. La agudeza visual decimal es reciproca al tamaño reconocido en C-Landolt (Lange et al., 2009).
El nivel de visión que ofrece las prótesis retinal es limitada. Algunos participantes refieren notables mejoras en la distinción de formas y objetos, les es útil para desplazarse con independencia y distinguir obstáculos, pero aun así describen las imágenes como “sombras en movimiento” (Humayun et al., 2016). Debemos considerar que independiente de la opción a elegir los afectados ya llevan mucho tiempo con discapacidad por lo que siempre será necesario el entrenamiento de rehabilitación para maximizar el impacto y darle sentido a la nueva información visual (Troy, 2015).
Aún no se puede predecir a que pacientes les será útil el mejorar la percepción de la luz, cuanto demorará la restauración de las habilidades y si esta será mantenida. Por lo tanto aún no hay una opinión generalizada sobre los beneficios de la visión artificial. Si sabemos que con la prótesis retinal el paciente tiene mayor habilidad de orientación, relación con el medio, sobrellevar obstáculos y mejora sus interacciones sociales pero no se encontraron estudios que comparara estas mejoras con respecto a las ayudas visuales ópticas (Humayun et al., 2016).
La retinosis pigmentaria representa un claro estado de alteración de la calidad de vida para quien la padece, representando así no solo una pérdida de autonomía por parte del individuo afecto sino también del núcleo familiar de este. Las técnicas de Rehabilitación Visual que se han desarrollado en los últimos años han sido en función de mejorar la autonomía y el desempeño del afectado en las labores cotidianas debido a que la edad de presentación es habitualmente en jóvenes lo cual genera una descompensación psicológica, no solo ameritando así la prestación de ayuda óptica sino también el apoyo multidisciplinario para el manejo de dicha afección, tanto para el paciente como para su familia (Kemper et al., 2012; Latham et al., 2017)
Entre las técnicas de rehabilitación diversos autores han podido plantear estrategias tales como las Terapias de Baja Visión, la cual resulta no solo de bajo costo sino además de gran utilidad para la ubicación temporal de estos pacientes. Así mismo, el uso de lupas y telescopios representan una alternativa que genera autonomía en caso donde la progresión de la enfermedad ha sido evidente, esto a un bajo costo, si lo comparamos con la prótesis retinal que se presenta como una gran alternativas ya que la misma posee utilidad en la mejora de localización y relación con el medio permitiendo además el uso de la binocularidad y reajuste de la imagen (Deemer et al., 2018; Farvardin et al., 2018).
En este mismo orden de ideas podemos señalar la prótesis Argus II la cual ha sido aprobada por la FDA, lo que valida de forma significativa su uso, sin embargo, numerosos informes han asegurado que las personas implantadas con estos dispositivos requieren un largo proceso de ajuste y capacitación, lo que refiere un desafío tanto para el paciente como para el familiar y el sistema de salud, debido a la inversión económica que esto representa (Ayton et al., 2014; Deemer et al., 2018; Farvardin et al., 2018).
Conclusiones
La Retinosis Pigmentaria representa una enfermedad que compromete significativamente la salud visual de quien la padece siendo un desafío para el equipo de salud y familiar, por tanto debemos siempre individualizar la prestación dada en cada caso, tomando en cuenta las condiciones del medio y núcleo familiar (Kempen et al., 2012; Trujillo et al., 2012).
Las diversas estrategias de Rehabilitación Visual juegan un papel significativamente importante en la terapéutica del paciente ya que permiten readaptación al medio, cuentan con un buen nivel de seguridad al no presentar contraindicaciones para su uso como en el caso explícito de las ayudas ópticas y asimismo han demostrado seguridad a largo plazo como las prótesis retinales (DaCruz et al., 2016; García et al., 2015; Stingl et al., 2015).
En este mismo orden de ideas es importante comprender que las ayudas ópticas corresponden a herramientas para maximizar el remanente visual, es decir, no tienen utilidad en los casos de pérdida completa de la visión, mientras que la prótesis retinal puede ser utilizada en cualquier etapa de la enfermedad siendo aún más provechosa en los estadios avanzados (DaCruz et al., 2016; Daschner et al., 2018; Farvardin et al., 2018; Lewis y Rosenfeld, 2016)
En este sentido es importante concluir que los test utilizados en la bibliografía consultada tanto para evaluar la calidad de vida como la calidad visual del paciente, no representan un criterio unificado por tanto no es posible establecer relaciones objetivas entre las diversas pruebas clínicas estudiadas.
AlSaqr, A. y Dickinson, C. (2016). A new measure for the assessment of visual awareness in individuals with tunnel vision. Clinical and Experimental Optometry, 100(1), 61-68.
Ayton, L., Blamey, P., Guymer, R., Luu, C., Nayagam, D., Sinclair, N., Shivdasani, M., Yeoh, J., McCombe, M., Briggs, R., Opie, N., Villalobos, J., Dimitrov, P., Varsamidis, M., Petoe, M., McCarthy, C., Walker, J., Barnes, N., Burkitt, A., Williams, C., Shepherd, R. y Allen, P. (2014). First-in-Human Trial of a Novel Suprachoroidal Retinal Prothesis. Plos one, 9(12).
Azoulay, L., Chaumet-Riffaud, P., Jaron, S., Roux, C., Sancho, S., Bergudo, N., Audo, I., Sahel, J. y Mohand-Said, S. (2015). Threshold Levels of visual Field and Acuity Loss Related to Significant Decreases in the Quality of life and Emotional States of Patients with Retinosis Pigmentaria. Ophthalmic Rsearch, 54:78-84.
Bach, M., Wilke, M., Wilhelm, B., Zrenner, E. y Wilke, R. (2010). Basic Quantitative Assessment of Visual Performance in Patients with Very Low Vision. Investigative Ophthalmology and Visual Science, 51(2), 1255-1260.
Brandli, A., Luu, C., Guymer, R. y Ayton, L. (2016). Progress in the clinical development and utillization of visión prostheses: an update. Eye and Brain, 2016(8), 15-25.
Bruijning, J., Nispen, R. y Rens, G. (2010). Feasibility of the Dutch ICF Activity Inventory: a pilot study. BMC Health Services Research, 10, 318.
Cohen, E. (2018). Retinal Prostheses. Webvision: The Organization of the Retina and Visual System (internet).PubMed PMID: 29697233
DaCruz, L., Dorn, J., Humayun, M., Dagnelie, G., Handa, J., Barale, P….Greenberg, R. (2016). Five-Year Safety and Performance Result from the Argus II Retinal Prosthesis System Clinical Trial. American Academy of Opthalmology, 123(10),2248-2254.
Daschner, R., Rothermel, A., Ralf, R.., Rudorf, S. y Stett, A. (2018). Functionality and Performance of the Subretinal Implant Chip Alpha AMS. Sensors and Materials,30(2),179-192.
Deemer, A., Bradley, C., Ross, N., Natale, D., Itthipanichpong, R., Werblin, F. y Massof, R. (2018). Low Vision Enhancement with Head- mounted Video Display System: Are We There Yet? Optometry and Vision Science, 95(9), 694-703.
Escobar Gómez, H., Vélez Álvarez, C. y Barrera Valencia, C. (2017). Ayudas externas para mejorar la independencia en personas con discapacidad visual. Revista Cubana de Oftalmología (online), 30(1).
Farvardin, M., Afarid, M., Attarzadeh, A., Johari, M., Mehryar, M., Nowroozzadeh, H., Rahat, F., Peyvandi, H., Farvardin, R y Nami, M. (2018). The Argus II Retinal Prosthesis Implantantion; From the Global To Local Successful Experience. Frontiers in Neuroscience, 12(584), 1-8.
García Martín, E., Gil Arribas, L. y Bambó Rubio, M. (2015). Retinosis Pigmentaria. Avances diagnósticos y terapéuticos. Revista de información e investigación oftalmológica de Laboratorios Thea.
Geruschat, D., Flax, M., Bianchi, M., Fisher, A., Goldschmidt, M., Fisher, L.,…Dorn, J. (2015). FLORA: Phase I development of a functional vision assessment for prosthetic vision users. Clinical and Experimental Optometry, 98(4).
Ghodasra, D., Chen, A., Arevalo, F., Birch, D., Branham, K., Coley,B.,…Jayasundera, T. (2016). Worlwide Argus II implantation: recommendations to optimize patient outcomes. BMC Ophthalmology, 16:52.
Grupo de trabajo de la Guía de Práctica Clínica para las Distrofias Hereditarias de Retina. Guía de Práctica Clínica para las Distrofias Hereditarias de Retina. Ministerio de Sanidad, Servicios Sociales e Igualdad. Servicio de Evaluación del Servicio Canario de la Salud (2017). Guía de Práctica Clínica en la SNS. Recuperado de http://enfermedades-raras.org/index.php/actualidad/actualidad-movimiento-asociativo/8185
Health Quality Ontario. (2016). Retinal prosthesis system for advanced retinosis pigmentaria: a health technology assessment. Ontario Health Technology Assessment Series (internet), 16(14), 1-63.
Humayun M., Eugene de Juan, J. y Dagnelie, G. (2016). A Quarter Century of Retinal Prosthesis Research and Development. American Academy of Ophthalmology, 123(10), S89-97.
Kempen, G., Ballemans, J., Ranchor, A., Van Rens, G. y Zijlstra, R. (2012). The impact of low vision on activities of daily living, symptoms of depression, feelings of anxiety and social support in community-living older adult seeking vision rehabilitation services. Quality of Life Research, 21, 1405-1411.
Lange, C., Feltgen, N. Junker, B., Schulze-Bonsel, K y Bach, M. (2009). Resolvion the clinical acuity categories “hand motion” and “counting fingers” using the Freiburg Visual Acuity Test (FrACT). Graefes Arch Clin Exp Ophthalmol, 247,137-142.
Latham, K., Baranian, M., Timmis, M. y Pardhan, S. (2015). Emotional Health of People with Visual Impairment Caused by Retinosis Pigmentaria. Plos One, 10(12).
Latham, K., Baranian, M., Timmis, M., Fisher, A. y Pardhan, S. (2017). Relative Difficulties of Daily Living Task with Retinosis Pigmentaria. Optometry and vision science, 94(3), 317-328.
Levinson, J., Joseph, E., Ward, L., Nocera, J., Pardue, M., Bruce, B. y Yan, J. (2017). Physical Activity and Quality of Life in Retinosis Pigmentaria (Research Article). Journal of Ophthalmology.
Lewis, P. y Rosenfeld, J. (2016). Electrical stimulation of the brain and the development of cortical visual prostheses: An historical perspective. Brain Research, 1630, 208-224.
Stingl, K., Bartz-Schmidt, K., Besch, D., Chee, C., Cottriall, C., Gekeler, F.,…Zrenner, E. (2015). Subretinal Visual Implant Alpha IMS- Clinical trial interim report. Vision Research, 111, 149-160.
Sugawara, T., Hagiwara, A., Hiramatsu, A., Ogata K., Mitamura, Y. y Yamamoto, S. (2010). Relationship between peripheral visual field loss and visión-related quality of life in patients with retinosis pigmentaria. Eye, 24, 535-539.
Troy, J. (2015). Visual Prostheses: Technological and Socioeconomic Challenges. Engieneering Sciences Press, 1(3), 288-291.
Trujillo, M., Pablo, S., Pinilla, P., Cuéllar, L., Valls, P., Ayuso, C…Serrano, P. (2012). Recomendaciones para el manejo terapéutico de la Retinosis Pigmentaria. Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad, Política Social e Igualdad. Servicio de Evaluación del Servicio Canario de la Salud. Informes de Evaluación de Tecnologías Sanitarias: SESCS N° 2010/03. Recuperado de http://www.gobiernodecanarias.org/sanidad/
Zhang, Q. (2016). Retinosis Pigmentaria. Progress and Perspective. Asia Pacific Journal Ophtalmolmology, 5(4), 265-271.
Consulta nuestra oferta formativa:
Busca
Visita nuestro perfil de Instagram
Últimas entradas
- 21 de abril de 2026
Modelos de cooperación internacional en optometría impulsados por la OMS
- 6 de febrero de 2026